Source: The Conversation – France in French (2) – By Alexandre Desparmet, Doctorant en Biologie Marine, Muséum national d’histoire naturelle (MNHN)
Les humains ainsi que bon nombre d’espèces vivantes ont besoin d’oxygène pour vivre. Pourtant cette molécule est chimiquement dangereuse, elle provoque ce que l’on appelle le « stress oxydant » (une altération des constituants de nos cellules comme les protéines ou l’ADN). Il faut donc pouvoir l’utiliser, mais également s’en protéger. Une nouvelle étude éclaire ces processus chez des microalgues.
La relation entre la vie et l’oxygène est loin d’être simple. Pour la comprendre, il faut remonter aux origines de la vie sur Terre, à l’époque archéenne (entre -4 milliards et -2,5 milliards d’années). Les océans existaient déjà, mais l’atmosphère contenait très peu, voire pas du tout, d’oxygène libre.
Certaines bactéries réalisaient déjà une photosynthèse dite anoxygénique qui, contrairement à celle des plantes et des algues actuelles, ne libère pas d’oxygène mais produit des composés soufrés.
Il y a environ 2,4 milliards d’années survient un tournant majeur : la Grande Oxygénation. L’oxygène commence à s’accumuler dans l’atmosphère grâce à l’activité de bactéries photosynthétiques (les cyanobactéries) capables de réaliser la photosynthèse oxygénique, le même processus que celui utilisé aujourd’hui par les plantes et les algues.
Cette accumulation d’oxygène transforme profondément la biosphère. Pour la première fois, une molécule extrêmement réactive est produite en grande quantité par des organismes vivants. L’oxygène peut oxyder et endommager les structures cellulaires des organismes qui n’y sont pas adaptés. La vie se trouve alors confrontée à un paradoxe : devoir composer avec une molécule qu’elle produit elle-même mais qui représente un danger pour la majorité des formes de vie existantes.
Cette transition provoque une crise biologique majeure. De nombreuses espèces anaérobies sont repoussées vers des milieux pauvres en oxygène, comme les sédiments ou les profondeurs marines. Parallèlement, certaines lignées développent des mécanismes capables de neutraliser l’oxygène, puis de l’utiliser comme source d’énergie. La respiration oxygénique, bien plus efficace que les métabolismes anaérobies, permet ainsi l’émergence de formes de vie plus complexes.

Cédric Hubas, CC BY
Le paradoxe de l’oxygène
Bien que souvent associé à la vie, l’oxygène demeure chimiquement dangereux et peut provoquer ce que l’on appelle le stress oxydant. En effet, le dioxygène peut générer des espèces réactives de l’oxygène (ERO) – superoxyde, peroxyde d’hydrogène ou radical hydroxyle – capables d’endommager protéines, lipides et ADN.
Tous les organismes aérobies (y compris les humains) possèdent donc des systèmes enzymatiques permettant de neutraliser ces molécules : superoxyde dismutases, catalases ou peroxydases. Sans ces mécanismes de défense, l’oxygène serait rapidement létal. La vie moderne repose ainsi sur un équilibre délicat : utiliser l’oxygène pour produire de l’énergie tout en limitant ses effets toxiques.
Longtemps considérées uniquement comme des sous-produits nocifs impliqués dans le vieillissement ou certaines maladies, les ERO sont aujourd’hui reconnues comme des molécules de signalisation participant à la régulation de nombreux processus cellulaires (prolifération cellulaire ou régulation de certains gènes par exemple). Leur rôle exact reste cependant encore largement inexploré.
Le stress oxydant dans les environnements naturels
Le stress oxydant ne concerne pas seulement les organismes humains : il affecte l’ensemble du vivant. Il apparaît lorsque la production d’ERO dépasse les capacités de défense de la cellule. Ce phénomène est particulièrement marqué dans des environnements soumis à de fortes variations de conditions physiques ou chimiques.
Ces milieux extrêmes comme la mer morte, le désert du Sahara ou certains déserts d’altitude recevant un fort rayonnement solaire, possèdent des conditions très salées, très sèches ou fortement irradiées, mais abritent pourtant une biodiversité étonnante. Des organismes spécialisés, appelés extrêmophiles, y prospèrent grâce à des adaptations physiologiques remarquables. La notion d’environnement extrême dépend donc toujours de l’organisme considéré.
Même des milieux plus familiers peuvent imposer des contraintes importantes. Nos zones côtières, par exemple, connaissent des fluctuations rapides de lumière. L’intensité lumineuse y varie fortement au cours de la journée, ce qui influence directement l’activité photosynthétique.
Les organismes photosynthétiques sont particulièrement exposés à ce problème, car la capture d’énergie lumineuse favorise la formation d’espèces réactives de l’oxygène. Ainsi, si la lumière est indispensable à la photosynthèse, un excès d’énergie lumineuse peut perturber l’équilibre cellulaire et favoriser la formation d’ERO. Les organismes doivent donc exploiter la lumière tout en se protégeant de ses effets potentiellement toxiques.
Les adaptations des microalgues aux variations journalières de lumière
Les diatomées, microalgues très abondantes dans les sédiments marins, ont développé plusieurs stratégies pour faire face à ces variations lumineuses. Des pigments protecteurs, notamment les xanthophylles, limitent la formation de radicaux libres. Les cellules peuvent également modifier l’organisation de leur appareil photosynthétique afin d’optimiser la capture de lumière tout en réduisant les dommages.
Ces microalgues possèdent aussi des photorécepteurs capables de détecter les variations lumineuses et de déclencher des réponses physiologiques rapides, comme l’activation de mécanismes de photoprotection ou l’expression de certains gènes.
L’une de leurs adaptations les plus remarquables est leur migration verticale dans le sédiment. Lorsque la lumière est modérée, les diatomées remontent vers la surface afin de maximiser la photosynthèse. Lorsque l’intensité devient trop forte, elles s’enfoncent légèrement dans le sédiment, comme pour se mettre à l’ombre. Ces déplacements sont synchronisés par une horloge circadienne interne qui permet d’anticiper les cycles jour-nuit.
ERO et diatomées : un dialogue plus complexe qu’on ne le croyait
Des travaux récents suggèrent que les espèces réactives de l’oxygène pourraient jouer un rôle plus actif qu’on ne le pensait. Au-delà de leur caractère potentiellement toxique, elles pourraient agir comme signaux déclenchant certaines réponses comportementales.
Notre dernière étude montre que les ERO participent notamment au contrôle de la migration verticale des diatomées, alors que l’on pensait jusqu’à présent que ces migrations servaient principalement à limiter leur production et leur accumulation au niveau cellulaire.
Deux mécanismes semblent donc se combiner : la migration permet de réduire l’exposition à des conditions génératrices d’ERO, mais ces mêmes molécules pourraient également agir comme signaux déclenchant la réponse lorsque leur concentration dépasse un certain seuil.
Ce système fonctionnerait ainsi comme un véritable dispositif de surveillance interne. Les variations du stress oxydant reflètent rapidement les changements de l’environnement et permettent aux cellules d’ajuster leurs réponses physiologiques et comportementales.
Les diatomées étant très diversifiées et largement distribuées à l’échelle globale, il est probable que ces capacités de détection, de traitement de l’information et de mise en place de réponses varient selon les espèces et le contexte environnemental. Cette diversité confère aux diatomées une forte capacité d’adaptation, jouant un rôle essentiel dans leur survie.
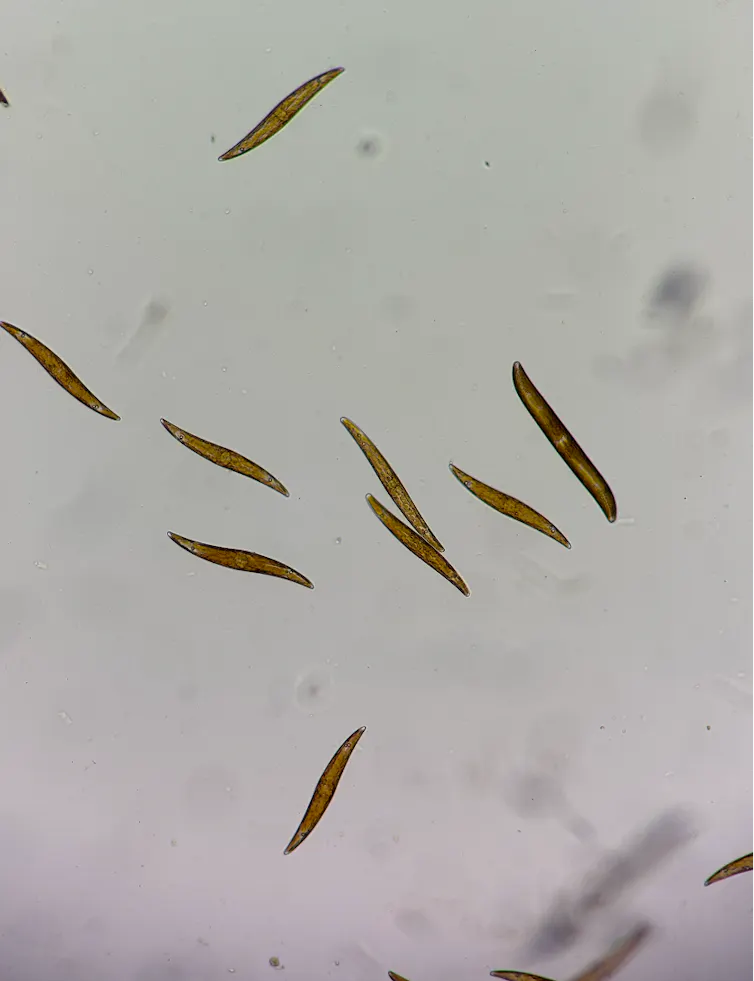
Alexandre Desparmet, Fourni par l’auteur
Ce travail montre, à travers un exemple frappant, que le vivant n’a pas seulement appris à se défendre contre l’oxygène et ses dérivés toxiques : il a aussi appris à les utiliser. Des déchets métaboliques oxygénés, autrefois considérés comme uniquement dangereux pour les cellules, peuvent devenir de véritables outils biologiques.
Cela rappelle que le rôle des ERO reste complexe et encore largement méconnu. Loin d’être de simples agents de stress, elles apparaissent aujourd’hui comme des molécules ambivalentes : des messagers subtils intégrés à des mécanismes fins de communication, d’adaptation cellulaire et de perception de l’environnement, notamment chez les diatomées.
Et comme souvent en sciences, ces découvertes ouvrent surtout de nouvelles questions… qui restent encore à explorer.
Nous remercions l’école doctorale DIVONA, la station marine de Concarneau (Finistère) et le laboratoire BOREA.
![]()
Alexandre Desparmet a reçu des financements de l’institut de l’Océan de l’Alliance Sorbonne Université.
Cédric Hubas a reçu des financements de l’institut de l’Océan de l’Alliance Sorbonne Université.
– ref. L’oxygène, cette molécule paradoxale, base de la vie et poison mortel : comment les microorganismes y font face – https://theconversation.com/loxygene-cette-molecule-paradoxale-base-de-la-vie-et-poison-mortel-comment-les-microorganismes-y-font-face-278706
