Source: The Conversation – France in French (2) – By Franck Martin, Directeur de recherche, Université de Strasbourg
Nous avons découvert le mécanisme biologique à l’origine des formes génétiques les plus fréquentes de deux maladies neurodégénératives : la maladie de Charcot et la Démence Fronto-Temporales. Ces nouvelles connaissances pourraient aider au développement de futures cibles thérapeutiques. Nos résultats viennent d’être publiés dans la revue Science.
La sclérose latérale amyotrophique (SLA), ou maladie de Charcot, est une pathologie neurodégénérative fatale, on estime à 3 ans l’espérance de vie à la suite du diagnostic de la maladie, elle touche environ 6000 personnes en France. La pathologie résulte de la destruction progressive des neurones en charge de commander les muscles, les motoneurones. La mort de ces neurones est à l’origine des troubles moteurs caractéristiques de la maladie (une paralysie complète des muscles des bras, des jambes et de la gorge entraînant une incapacité à marcher, manger, parler ou même respirer qui s’installe progressivement).
Les causes de cette pathologie sont très variées. 10 % des cas de SLA sont d’origine génétique, contre 90 % de cas sporadiques, c’est-à-dire sans cause identifiée. Dans le cas de la forme génétique, la cause la plus fréquente est un défaut au niveau d’un gène spécifique (C9ORF72) qui provoque la synthèse de protéines toxiques qui entraînent la mort des motoneurones.
Ce gène contient des séquences qui sont anormalement répétées et qui portent une information génétique erronée. La traduction de ce défaut génétique conduit à la fabrication de protéines aberrantes (car elles ne devraient pas exister) et neurotoxiques. Notre découverte a permis de comprendre que cette synthèse de protéines toxiques est seule responsable de la pathologie. En bloquant spécifiquement la fabrication de ces dernières, nous avons réussi à enrayer la dégénérescence des motoneurones et de ce fait empêcher l’apparition de la maladie.
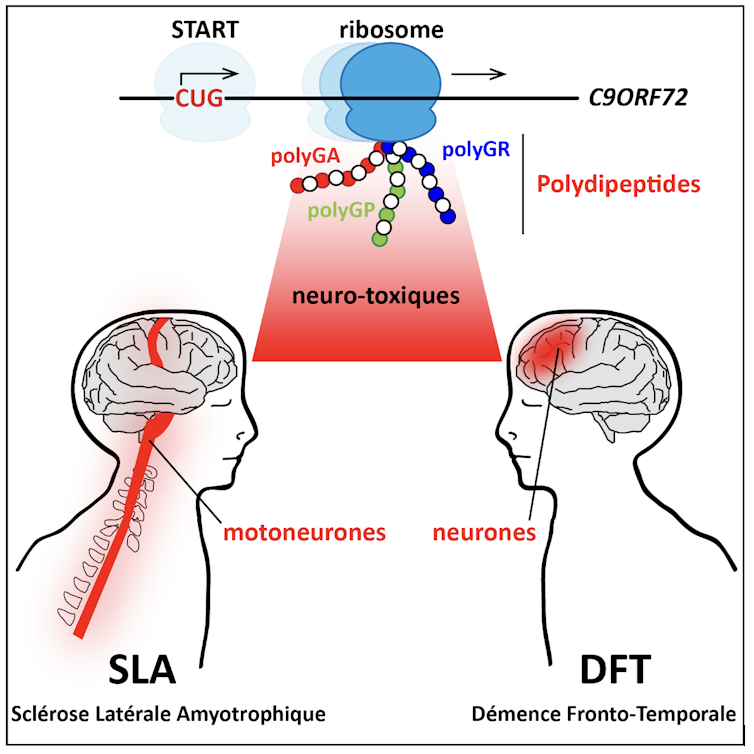
Fourni par l’auteur
Comment cette découverte a-t-elle pu être réalisée ?
Nous avons dans un premier temps reproduit, in vitro, la synthèse de protéines toxiques responsables de la mort des motoneurones. Ces protéines sont produites par le ribosome des cellules à partir du gène C9ORF72. Dans toutes les cellules, les protéines sont produites par les ribosomes. Ces machineries reconnaissent des sites spécifiques de l’ARN, c’est-à-dire des séquences particulières. Une fois fixé, le ribosome va lire l’ARN et le traduire en protéine. Si le ribosome ne reconnaît pas ce site particulier, la synthèse de protéines est impossible.
Grâce à ces expériences, nous avons pu identifier le site de démarrage du ribosome. En introduisant une simple mutation ponctuelle (remplacement d’une seule base par une autre) dans ce site au niveau du gène C9ORF72, la synthèse des protéines toxiques est totalement éteinte. Nous avons confirmé ces résultats dans des cellules, puis chez des souris.
La suite de notre travail a consisté à utiliser ces connaissances pour corriger le gène C9ORF72 dans des motoneurones de patients SLA (cultivés en laboratoire). Grâce à la technologie des « ciseaux moléculaires » CrispR-Cas9, le site de démarrage du ribosome a été modifié, cette seule modification est suffisante pour éteindre totalement la synthèse toxique dans ces motoneurones et restaurer leur durée de vie.
En quoi cette découverte est-elle importante ?
La SLA, comme la plupart des maladies neurodégénératives, sont des maladies qui sont déclenchées par des causes multifactorielles. Ceci rend le traitement de ces pathologies extrêmement compliqué. Nos recherches ont permis de caractériser le mécanisme moléculaire déclenchant la pathologie et ont conduit à l’identification précise de la cause de la SLA dans la forme la plus fréquente de la maladie, ce qui représente environ 8 % des cas. La découverte du site de démarrage de la synthèse de protéines toxiques pour les motoneurones est primordiale. Ce site de démarrage est maintenant une cible thérapeutique nouvelle pour le développement de nouveaux traitements.
Quelles sont les suites de ces travaux ?
L’objectif de nos recherches à venir est de cibler spécifiquement le site de démarrage de la synthèse de protéines neurotoxiques produites à partir du gène C9ORF72 afin d’empêcher la mort prématurée des motoneurones chez les patients SLA.
Ceci revêt une importance capitale pour les malades atteints de la SLA pour laquelle il n’existe pas de traitements mais aussi d’autres maladies neurodégénératives comme la Démence Frontotemporale (DFT) dont plus de la moitié des formes familiales est également due à ces même répétitions de séquences dans le gène C9ORF72. Nos recherches ouvrent donc de nouvelles pistes de recherche pour la mise au point de traitements thérapeutiques ciblant la synthèse de protéines neurotoxiques chez les patients SLA et DFT.
Tout savoir en trois minutes sur des résultats récents de recherches commentés et contextualisés par les chercheuses et les chercheurs qui les ont menées, c’est le principe de nos « Research Briefs ». Un format à retrouver ici.
![]()
Franck Martin a reçu des financements de l’ANR, la FRM, l’ARSLA, l’AFM Telethon et France Alzheimer
– ref. Maladie de Charcot : le mécanisme à l’origine de la forme génétique de la pathologie a été découvert – https://theconversation.com/maladie-de-charcot-le-mecanisme-a-lorigine-de-la-forme-genetique-de-la-pathologie-a-ete-decouvert-275265
