Source: The Conversation – France in French (3) – By Dominique Costagliola, Épidémiologiste et biostatisticienne, directrice adjointe de l’Institut Pierre Louis d’Épidémiologie et de Santé Publique (Sorbonne Université/Inserm), directrice de recherches, Inserm
Épidémiologiste et biostatisticienne, membre de l’Académie des Sciences, Dominique Costagliola est directrice de recherche émérite à l’Inserm. Cette figure de la recherche contre le VIH fait le point pour The Conversation sur la situation de l’épidémie en France, et revient sur les conséquences, au niveau mondial, du retrait des aides états-uniennes.
The Conversation France : En France, combien de personnes vivent actuellement avec le VIH ?
Dominique Costagliola : En France, en 2023, selon les estimations de Santé publique France, 181 000 personnes vivaient avec le VIH.
Soulignons que Santé publique France a déployé l’an dernier une nouvelle méthode d’estimation de l’incidence du VIH en France et d’autres indicateurs clefs, les chiffres de ces deux dernières années ne doivent donc pas être directement comparés aux chiffres plus anciens.
En ce qui concerne les nouveaux diagnostics annuels, le chiffre le plus élevé dans l’Hexagone est relevé en Île-de-France (environ 162 nouveaux cas par million d’habitants), suivi par la région Provence-Alpes-Côte d’Azur (64) et le Centre-Val de Loire (55).
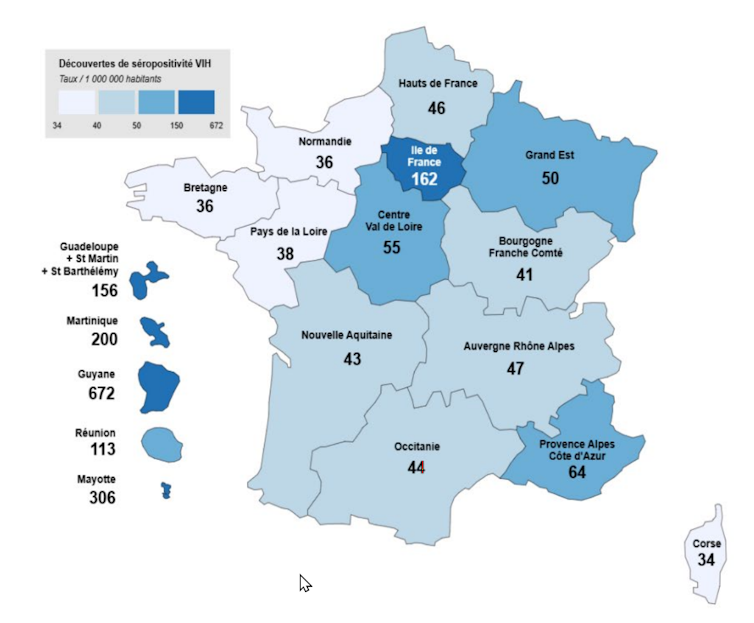
France, 2024.
Santé publique France, DO VIH, données au 30 juin 2025 corrigées pour tenir compte de la sous-déclaration, des délais de déclaration et des déclarations incomplètes
Les taux de découverte de séropositivité annuels sont particulièrement élevés dans les départements et régions d’outre-mer. Dans les Antilles, on dénombrait 200 nouveaux diagnostics par million d’habitants à la Martinique et 156 pour l’ensemble Guadeloupe, Saint-Martin et Saint-Barthélemy. À Mayotte, ce taux est de 306. En Guyane, il monte à 672. Cela semble peu en nombre de personnes, mais rapporté à la population, c’est conséquent.
Dans les 30 pays de l’Union européenne, les nouveaux diagnostics se situent en moyenne à 5,3 pour 100 000 habitants et par an (données ECDC/OMS de 2023). Quand on regarde plus en détail, on constate que la situation varie de 2,1 nouveaux diagnostics pour 100 000 habitants en Slovénie et en Autriche, jusqu’à 17,6 à Chypre ou 21 à Malte. En France, en 2024, on est à 7,5 nouveaux diagnostics pour 100 000 habitants. Ce niveau est relativement proche de celui des pays voisins (9,5 en Belgique, 8,8 au Portugal, 6,6 en Espagne, 4 en Italie, 3,9 en Allemagne – données 2023).
TCF : Que peut-on dire de la dynamique de l’épidémie dans notre pays ?
DC : Les estimations d’incidence de Santé publique France indiquent une stabilisation dans toutes les populations considérées (personnes hétérosexuelles nées à l’étranger, personnes hétérosexuelles nées en France, HSH nés en France, HSH nés à l’étranger, usagers de drogues injectables, personnes trans contaminées par rapports sexuels).
Cette tendance tranche avec les évolutions contrastées qui avaient été observées entre 2012 et 2021. Sur cette période, l’incidence a baissé en France, cependant cette baisse se voyait surtout chez les hommes ayant des relations sexuelles avec les hommes (HSH) nés en France.
Depuis 2022, le nombre de nouveaux diagnostics ne diminue plus dans cette population, ce qui est une source de préoccupation. À l’inverse, alors qu’il augmentait chez les HSH nés à l’étranger sur la même période, il se stabilise depuis deux ans.
Les chiffres révèlent que la baisse de l’incidence chez les HSH était modeste de 2012 à 2015 Le changement observé est probablement en partie lié à la modification du des recommandations de prise en charge. À partir de 2013, ces dernières ont préconisé de « mettre en place un traitement antirétroviral chez toute personne vivant avec le VIH », autrement dit dès le diagnostic. Auparavant, quand un individu était diagnostiqué, il n’était pas immédiatement mis sous traitement antirétroviral (on attendait que son taux de lymphocytes T CD4 – les cellules immunitaires qui sont progressivement détruites par le virus – diminue).
Ce changement de paradigme a eu un impact sur la circulation de la maladie. En effet, la charge virale des personnes sous traitement est contrôlée. En conséquence, elles ne transmettent pas le virus.
L’accentuation de la baisse à partir de 2016 peut quant à elle s’expliquer par la mise à disposition de la PrEP (prophylaxie pré-exposition), innovation qui s’est répandue progressivement, essentiellement dans ce groupe.
Pour mémoire, cette approche consiste à fournir un traitement antirétroviral préventif aux personnes non encore infectées par le VIH mais à risque d’être exposées, afin de prévenir la contamination. Il s’agit d’une mesure complémentaire aux autres moyens de prévention. Concrètement, les individus concernés prennent des comprimés, quotidiennement ou à la demande (dans ce cas, avant et après une prise de risque).
TCF : La pandémie de Covid-19 a-t-elle eu un impact sur l’épidémie de VIH en France ?
DC : On constate qu’en 2020, le nombre de nouveaux diagnostics a diminué de façon importante. On peut probablement y voir en partie l’effet de la pandémie de Covid-19 : on dépistait moins à cette époque, en raison des perturbations du système de santé. Le fait qu’il y a eu à cette époque davantage de distanciations sociales qu’à l’accoutumée a peut-être aussi contribué à limiter la transmission.
Depuis ce plus bas niveau, estimé à 4 500 nouveaux cas environ en 2020, une remontée du nombre de nouveaux diagnostics a été observée. Elle pourrait être simplement due à la reprise de l’activité de dépistage, voire à son augmentation. En effet, depuis 1er janvier 2022, il est possible d’effectuer un dépistage du VIH dans tous les laboratoires d’analyses biologiques de France, sans ordonnance.
(ce dispositif a été étendu en septembre 2024 à quatre autres infections sexuellement transmissibles (le virus de l’hépatite B et les bactérie_ Treponema pallidum (responsable de la syphilis), Neisseria gonorrhoeae (gonorrhée) et Chlamydia trachomatis _(chlamydiose). Depuis cet élargissement, Santé publique France a constaté un doublement du nombre mensuel de 15-24 ans qui se sont fait tester pour le VIH (la prise en charge est de 100 % pour les moins de 26 ans), NDLR)
En 2024, 8,5 millions de tests VIH ont été réalisés, lesquels ont mené à la découverte de 5100 nouveaux diagnostics de séropositivité. Ce chiffre semble indiquer une tendance à la stabilisation, mais il faudra voir si celle-ci se confirmera dans les années à venir.
TCF : Qui sont ces personnes, et sait-on comment elles ont été contaminées ?
DC : L’âge au moment du diagnostic est très variable selon la population considérée. Chez les personnes hétérosexuelles, la part des seniors (50 ans et plus) est nettement plus importante que dans les autres populations. Parmi les 5100 personnes nouvellement diagnostiquées en 2024, 44 % étaient nées en France, et 56 % à l’étranger.
Les deux modes principaux de contamination sont les rapports hétérosexuels (53 % des cas en 2024), et les rapports sexuels entre hommes (42 % des diagnostics). Les autres modes de contamination sont beaucoup moins fréquents (le partage de matériel d’injection dans le cas des usagers de drogues représentait 1 % des diagnostics, les contaminations mère-enfant, 1 % également, les contaminations sexuelles de personnes trans 2 %).
On remarque qu’en 2024, 47 % des personnes nées à l’étranger qui ont découvert leur séropositivité en France se sont avérées avoir été contaminées après leur arrivée dans notre pays.
Les personnes vivant avec le VIH sans le savoir constituent une source particulière de préoccupation. Selon Santé publique France, elles étaient environ 9675 fin 2024. Si ce chiffre est en baisse de 10 % par rapport à 2023, il nécessite de poursuivre les efforts en matière de dépistage.
TCF : C’est un point important, car pour limiter la transmission, il est essentiel de raccourcir le délai qui s’écoule entre le moment où un individu est contaminé est celui où il est diagnostiqué…
DC : En effet, car si l’on ne sait pas que l’on est infecté, on ne va pas prendre de précaution, et donc on va être susceptible de contaminer d’autres personnes. À l’inverse, les données de la littérature scientifique démontrent que quand les gens connaissent leur séropositivité, ils prennent moins de risques.
Par ailleurs, une fois diagnostiqué, on reçoit un traitement qui permet de contrôler la charge virale. À partir de ce moment, on ne transmet plus le virus.
Donc plus tôt on se fait dépister, plus le risque de transmettre le virus est limité, car ce sont plutôt les personnes qui ignorent leur statut qui sont à la source des nouvelles contaminations.
Enfin, plus les traitements sont initiés tôt, meilleures sont les chances de parvenir à contrôler le virus et à restaurer le système immunitaire.
TCF : À l’heure actuelle, quel est le délai entre la contamination et le diagnostic ?
DC : Santé publique France l’estime à 1,7 an en médiane, mais il varie beaucoup selon la situation considérée.
Ainsi, ce délai est d’environ 3 ans pour les hommes hétérosexuels nés à l’étranger. Il est d’un peu plus de 2 ans et demi pour les femmes hétérosexuelles nées à l’étranger, et d’un peu moins de 2 ans et demi pour les hommes hétérosexuels nés en France. Pour les hommes ayant des relations sexuelles avec les hommes nés en France, il est légèrement inférieur à un an (et légèrement supérieur à un an pour les HSH nés à l’étranger et les personnes trans contaminées par rapport sexuel).
On sait aussi que le risque de contamination est plus élevé chez les personnes précaires, qui ont moins de possibilités de s’occuper correctement de leur santé. Il s’agit là d’un obstacle à surmonter pour être capable de gérer correctement l’épidémie.
TCF : À partir de 2015, la prophylaxie préexposition (PrEP) a également été intégrée aux recommandations officielles. Que peut-on en dire ?
DC : L’ANSM a établi en novembre 2015 une recommandation temporaire d’utilisation (RTU) du Truvada pour la PrEP, devenue effective en janvier 2016. Ce médicament est une association entre deux molécules qui inhibent des enzymes indispensables au bon fonctionnement du VIH (ténofovir – ou TDF – et emtricitabine – ou FTC).
Selon les données du Groupement d’Intérêt scientifique EPI-PHARE, qui depuis 2017 assure le suivi de l’évolution de l’utilisation de Truvada ou de ses génériques en France dans le cadre d’une PrEP, durant le premier semestre 2025, 67505 personnes utilisaient effectivement la PrEP, que ce soit en initiation ou en renouvellement. Les personnes qui y ont eu recours en France entre le 1er janvier 2016 et le 30 juin 2025 sont principalement des hommes (94 %), âgés de 33 ans en médiane. La grande majorité (69 %) résidait dans des communes appartenant à des unités urbaines de plus de 200 000 habitants.
On ne sait pas dans quelle mesure la PrEP couvre correctement les populations les plus à risque, mais on peut supposer que ce n’est sans doute pas suffisant, en tout cas pour la prévention.
TCF : D’autres médicaments soulèvent de grands espoirs pour limiter la transmission : les PrEP injectables. De quoi s’agit-il, et où en est-on en France ?
DC : À l’heure actuelle, en France, la PrEP repose sur l’association TDF/FTC. Ces molécules sont fabriquées par plusieurs laboratoires, sous forme générique. Elles sont donc bon marché.
À côté de ces PrEP, qui se prennent sous forme de cachets, sont développées des PrEP injectables, comme le cabotégravir (du laboratoire VIIV HEALTHCARE – qui est également utilisable en traitement, en bithérapie).
En PrEP, cette molécule requiert une injection tous les deux mois, en intramusculaire. Elle dispose d’une autorisation de mise sur le marché au niveau européen, mais sa commercialisation en France reste en suspens, car les discussions sur son remboursement n’ont pas encore abouti. Une étude est en cours pour évaluer le service médical rendu par rapport à la PrEP TDF/FTC.
Une autre PrEP injectable, le lénacapavir (laboratoire Gilead), a fait beaucoup parler d’elle en raison de la formidable efficacité dont elle a fait montre lors des essais cliniques : durant ces derniers, aucune infection n’a été détectée. Certes, les échantillons étaient de taille modeste, mais ça n’en est pas moins impressionnant.
Autre intérêt du lénacapavir : cette PrEP ne requiert qu’une injection tous les six mois. Elle a d’ailleurs été officialisée par l’OMS en tant qu’option supplémentaire dans ses recommandations de PrEP.
TCF : En ce qui concerne les traitements antirétroviraux, où en est-on ? Sont-ils satisfaisants ?
DC : Aujourd’hui, nous disposons en France de traitements qui permettent de prendre en charge toutes les situations cliniques, y compris les personnes porteuses de virus très résistants. On retrouve ici encore le lénacapavir, mentionné précédemment, qui dispose d’une indication dans de tels cas de figure. L’efficacité de cette molécule repose sur son mode d’action totalement nouveau (elle interagit avec les protéines de la capside du VIH-1, bloquant différentes étapes du cycle de réplication viral).
De nouvelles molécules sont en cours de développement, notamment les traitements injectables avec seulement quelques injections par an, ou dans de nouvelles familles ciblant de nouveaux gènes du virus ou dans les familles existantes.
Ces traitements, bien qu’ayant un coût et devant être pris à vie, permettent néanmoins aux personnes vivant avec le VIH d’avoir une espérance de vie qui se rapproche beaucoup de celle de la population générale. À condition que le diagnostic soit fait suffisamment tôt, afin de contrôler rapidement la charge virale, avant que les taux de LT CD4 ne diminuent trop.
Or, en 2024, environ 26 % des gens étaient encore diagnostiqués à un stade avancé de la maladie, autrement dit avec un taux de LT CD4 inférieur à 200 par mm3 de sang (ce qui correspond à un risque élevé de développer des maladies), ou bien à un moment où ils avaient déjà une pathologie opportuniste classant au stade Sida (résultant de l’immunodépression induite par l’infection). Dans cette situation, le temps pour réussir à récupérer des taux de LT CD4 supérieurs à 500 et diminuer l’inflammation qui est induite par l’infection sera très long.
Le fait d’avoir été immunodéprimé et de l’être resté longtemps, soit en raison d’un diagnostic tardif soit parce que l’on a été infecté avant la mise à disposition des traitements ou avant la recommandation universelle de traitement peut avoir des conséquences à long terme sur le risque de pathologies, telles que les cancers ou les maladies cardiovasculaires.
C’est aussi le cas lorsqu’on a été exposé aux premières générations d’inhibiteurs nucléosiques de la reverse transcriptase (AZT, DDI ou D4T) ou d’inhibiteurs de protéase (lopinavir)
TCF : quelle proportion de patients cela représente-t-il ?
DC : On sait qu’à l’heure actuelle, environ un quart des gens qui sont dans les files actives (une file active se définit comme le nombre de patients différents vus en consultation au moins une fois dans l’année, NDLR) ont été diagnostiqués avant 1996. Donc avant l’avènement des trithérapies.
Les trois quarts restants ont majoritairement été diagnostiqués avant 2013 (autrement dit avant la recommandation universelle de traitement). Les histoires de ces patients diffèrent donc en fonction du contexte historique de leur prise en charge.
Il faut cependant souligner qu’en France, 97 % des gens sont traités et ont une charge virale contrôlée. À condition de ne pas arrêter le suivi, bien entendu. Or, un certain nombre de personnes, qu’on a du mal à évaluer, arrête parfois leur prise en charge.
TCF : Nous sommes en 2025, et les recherches sur un potentiel vaccin sont toujours en cours. Pourquoi est-ce si compliqué ? Qu’apporterait un vaccin ?
DC : Si efficaces que soient les traitements, ils doivent être pris à vie, et ne sont pas parfaits (en raison de certains effets secondaires notamment). Par ailleurs, ils coûtent cher. Les trithérapies qui sont les plus populaires à l’heure actuelle ne sont pas encore disponibles sous forme générique. Un vaccin abordable qui conférerait une protection de long terme permettrait de diminuer drastiquement les nouvelles infections et le coût de leur prise en charge.
La difficulté est que pour développer un vaccin qui fonctionne contre un micro-organisme, il faut trouver un moyen d’activer les défenses que notre corps met en œuvre spontanément face à lui. Or, le VIH est précisément problématique parce qu’il échappe au système immunitaire, et le dégrade…
On ne connaît que quelques cas exceptionnels de personnes qui ont développé une immunité naturelle face à ce virus. Étant donnée la rareté de tels individus, monter des projets de recherche est très compliqué. Et ce, d’autant plus que la généralisation des traitements empêche d’en découvrir de nouvelles.
Soulignons cependant que la difficulté à mettre au point un vaccin ne signifie pas qu’il faille abandonner les recherches. On ne sait jamais ce qui pourrait en sortir, comme l’illustre l’histoire des vaccins à ARNm : lorsque quelques équipes ont commencé, il y a vingt ans, à envisager d’utiliser cette molécule comme vaccin, beaucoup de gens leur ont ri au nez, en raison des difficultés techniques à surmonter… On sait comment les choses ont fini par tourner.
Ce point dépasse le cadre de la lutte contre le VIH. Les politiques de la recherche doivent offrir aux scientifiques une marge de manœuvre afin qu’ils puissent travailler également sur des sujets non ciblés, aux côtés de ce qui semble plus immédiatement prometteur ou « productif ». Adopter un tel équilibre – raisonné – est garant d’un financement de la recherche sain. Et il faut soutenir les jeunes scientifiques, pour qu’ils puissent réaliser pleinement leur potentiel et atteindre leur point de capacité maximum !
TCF : À propos de financements, l’administration Trump, aux États-Unis, a brutalement coupé de nombreuses subventions dédiées à la lutte contre le VIH. Quelles en sont les conséquences ?
DC : Le gouvernement des États-Unis a décidé de faire disparaître USAID (United States Agency for International Development), l’agence autonome des États-Unis pour l’aide internationale, créée en 1961.
Le programme PEPFAR (President’s Emergency Plan for AIDS Relief, lancé en 2003), plan d’aide d’urgence destiné à la lutte contre le VIH, a finalement été maintenu en partie après une suspension, mais son fonctionnement a été fortement impacté.
Il faut savoir que dans certains pays à revenus limités, l’infrastructure de soins et les traitements étaient financés à 80 %, voire jusqu’à 100 %, à la fois par l’USAID et par PEPFAR, qui finançait les antirétroviraux. Soulignons à ce sujet qu’il ne s’agit pas d’avoir les traitements, il faut également les infrastructures pour les distribuer, faire les tests de dépistages, assurer le suivi des patients… C’est ce que permettait USAID. Son arrêt brutal a totalement désorganisé les services de soins pour les personnes vivant avec le VIH.
Le retrait des financements américains a aussi eu des conséquences sur l’agence ONUSIDA (UNAIDS en anglais), l’agence de l’ONU dédiée à la lutte contre le VIH : ses services aux communautés ont dû être fortement réduits (sur 70 bureaux nationaux ayant fait remonter des données, 40 % ont indiqué avoir dû cesser ces activités).
Le devenir de PEPFAR, qui a été sauvé par le Congrès des États-Unis en juillet, reste peu clair. En juillet 2025, les responsables de l’ONUSIDA estimaient que « six millions de nouvelles infections par le VIH et quatre millions de décès supplémentaires liés au sida pourraient survenir entre 2025 et 2029 si les services de traitement et de prévention du VIH soutenus par les États-Unis s’effondrent complètement ».
Les auteurs d’une étude publiée dans la revue Lancet en mai 2025 ont par ailleurs estimé qu’une réduction de 24 % de l’aide internationale, combinée à l’arrêt du soutien du PEPFAR, dans les pays à revenus faibles et intermédiaires pourrait entraîner entre 4,43 et 10,75 millions de nouvelles infections par le VIH, ainsi qu’entre 0,77 et 2,93 millions de décès supplémentaires liés au VIH sur la période 2025 et 2030, par rapport au statu quo. Si PEPFAR revenait à un niveau équivalent à celui d’avant la crise, ces chiffres pourraient être ramenés respectivement 0,07 à 1,73 million de nouvelles supplémentaires et 0,005 à 0,061 million de décès.
Ces coupes menacent aussi la recherche, notamment en Afrique du Sud, qui figure parmi les pays les plus touchés. Il s’agit non seulement l’un des pays où l’incidence est la plus élevée, mais aussi l’un de ceux qui comptent la plus grande expertise en matière d’essais cliniques…
Il faut noter que la baisse de l’aide américaine n’est pas la seule en cause, même si sa brutalité a limité les capacités de réaction. Dans de nombreux pays riches, dont la France, l’aide au développement est en baisse. Dans ce contexte, les inquiétudes sur la reconstitution du Fonds mondial sont importantes.
Cette situation doit nous faire réfléchir sur le manque de sécurité que représente un mode de financement des systèmes de soin qui repose quasi exclusivement sur un seul bailleur. Il s’agit là d’une question qui dépasse le seul cadre de la lutte contre le VIH. C’est un enjeu majeur en matière de santé publique.
![]()
Dominique Costagliola est membre de l’association AIDES et de son conseil d’administration. Au cours des 5 dernières années, elle a fait un exposé non rémunéré en 2022 dans le cadre d’une réunion organisée avec le soutien de Pfizer sur “Recherche Clinique dans l’urgence, Pourquoi, Comment ? “. Au cours des 5 dernières années son laboratoire a reçu 1 contrat de recherches de Janssen sur l’utilisation de la rilpivirine en France.
– ref. Journée mondiale de lutte contre le sida : Où en est l’épidémie de VIH en France ? – https://theconversation.com/journee-mondiale-de-lutte-contre-le-sida-ou-en-est-lepidemie-de-vih-en-france-270584
