Source: The Conversation – (in Spanish) – By Gemma Marfany Nadal, Profesora Catedrática de Genética, Universitat de Barcelona
Una noche, Tomás se dio cuenta que algo fallaba. Había salido incontables veces con sus amigos a dar una vuelta por los caminos fuera del pueblo, un pueblo demasiado pequeño como para que sus voces alegres pasaran desapercibidas en la quietud nocturna.
En aquellos caminos no había farolas: solo la luz de la luna les alumbraba. Hasta entonces esto no le había supuesto ningún problema. Pero de repente se dio cuenta de que no podía distinguir bien los bordes del camino. Se paró, dudando y tratando de encontrar referencias, pero eran borrosas en los lados de su visión. Sin saberlo, Tomás acababa de detectar los primeros síntomas de una retinosis pigmentaria: la pérdida de visión en luz tenue, también llamada ceguera nocturna.
Una de cada 4 000 personas en todo el mundo sufre retinosis pigmentaria. Y si añadimos el resto de enfermedades genéticas raras que afectan a la visión, la prevalencia puede llegar hasta 1 de cada 2 000 personas.
Cómo vemos colores y luces
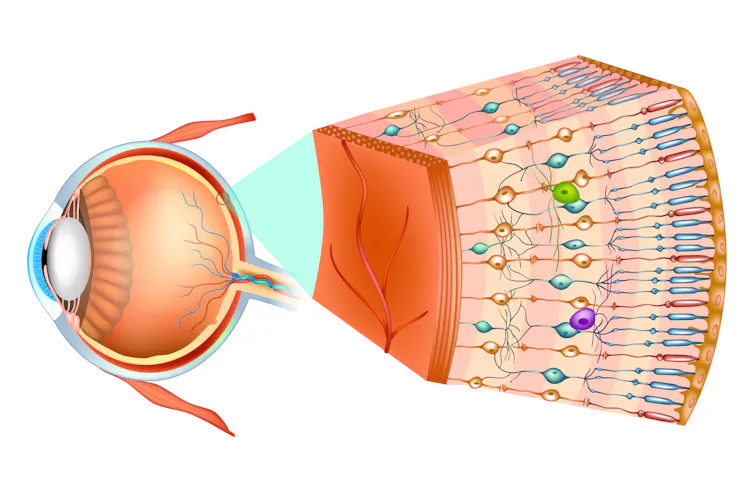
La retina es el tejido neurosensorial que tapiza el fondo de nuestro ojo. Se forma durante el desarrollo como un saliente del sistema nervioso central, que se abre en forma de copa hacia el exterior para diferenciarse en distintas capas neuronales perfectamente distribuidas y conectadas entre ellas.
La capa neuronal retiniana más alejada de la entrada de luz es la capa de células fotorreceptoras, conos y bastones, que pueden excitarse con el impacto de un único fotón. Estas células son las encargadas de recibir el estímulo luminoso y transformarlo en estímulo químico, primero, y en eléctrico, después.
En total, la retina humana posee alrededor de 120 millones de bastones y unos 7 millones de conos.
Los bastones son las células fotorreceptoras encargadas de la visión en luz tenue, porque se estimulan con fotones (partículas) de luz de baja intensidad. Concretamente estos fotones excitan a la rodopsina, la molécula sensible a la luz.
Los bastones no pueden percibir el color: solo ven en blanco y negro. Todo lo contrario que los conos, que expresan opsinas que responden a fotones de alta intensidad. Eso los convierte en responsables de la visión en color.
Sakurra/Shutterstock
Una distribución desigual
Los bastones están repartidos por toda la retina, mientras que los conos se acumulan sobre todo en la mácula, en la zona central de la retina (fóvea). Esa alta densidad de conos proporciona agudeza visual, o lo que es lo mismo, una extrema sensibilidad al contraste.
De noche, con luz tenue, solo pueden activarse los bastones. Por eso cuando oscurece vemos en blanco y negro y no podemos leer, aunque tenemos buena visión periférica.
Pero si en medio de la oscuridad encendemos una linterna, con un haz intenso de luz, o nos colocamos bajo una farola, los fotones de alta intensidad activan a los conos. Y empezamos a percibir colores y detalles como en pleno día.
Es el cerebro el que interpreta qué vemos
En la retinosis pigmentaria, debido a mutaciones en genes importantes para la función de los bastones, estas células se alteran, dejan de funcionar y acaban “suicidándose”: es lo que se conoce como muerte celular programada. Como consecuencia, se inicia y una pérdida de bastones que progresa paulatinamente, de fuera hacia dentro.
En la retina de Tomás, el protagonista de nuestra historia inicial, la enfermedad estaba avanzando sin que él lo supiera hasta que se traspasó un umbral en que la pérdida de bastones ya afectó a la percepción visual. La visión nocturna quedó afectada. Y empezó a experimentar lo que se conoce como visión en túnel: le costaba localizar los objetos circundantes pero aún podía leer y percibir detalles porque en la mácula los conos seguían siendo funcionales.
A largo plazo, la progresión de la enfermedad acaba afectando también a los conos, provocando una ceguera total.
Los primeros síntomas aparecen en la adolescencia tardía
Los pacientes con retinosis pigmentaria suelen empezar a notar los síntomas en la adolescencia tardía o en la etapa adulta. Pero cuando hay mutaciones que afectan a genes estructurales de los fotorreceptores o durante el desarrollo, la enfermedad puede aparecer durante la infancia, como sucede en la amaurosis congénita de Leber. Otra enfermedad congénita, la acromatopsia, se caracteriza porque los afectados solo pueden ver en blanco y negro. El mundo se percibe en tonos de gris, literalmente.
En otras patologías raras de la retina, como es el caso de la enfermedad de Stargardt, las mutaciones afectan genes relevantes para los conos o la mácula, que son los primeros que mueren. Eso permite que los pacientes vean con poca luz, pero sin embargo sean incapaces de leer los detalles de un rostro humano.
En busca de tratamientos
Actualmente, no existen tratamientos aprobados que detengan la degeneración de la retinosis por completo.
Para el diseño y aplicación de terapias avanzadas específicas, es imprescindible llevar a cabo investigación básica de los procesos genéticos, bioquímicos y celulares que se alteran cuando aparecen mutaciones en genes de la retina.
Aquí es donde entra en juego la biotecnología, que permite analizar modelos de la enfermedad, bien sea generando ratones avatar (con la dolencia) o mediante organoides humanos de retina, lo más parecido a una retina humana pero en una placa de Petri.
Partiendo de ahí podremos desarrollar tratamientos de medicina de precisión dirigida a enfermedades causadas por genes o mutaciones concretas –como Luxturna, para mutaciones del genRPE65–. Pero también terapias en las que el objetivo es la supervivencia de los fotorreceptores, sin focalizarse en un gen o mutaciones concretos: es lo que se conoce como terapias “agnósticas”.
Dos caminos para tratar y, quizás, incluso curar a Tomás y otros pacientes que, como él, tienen enfermedades raras hereditarias de la retina.
![]()
Gemma Marfany Nadal recibe fondos del Ministerio de Ciencia e Innovación para financiar investigación básica. Soy jefa de la unidad U-718 del CIBERER-ISCIII (Centro de Investigación Biomédica en Red de Enfermedades Raras). Soy miembro de la Comissió Nacional de Bioètica d’Andorra.
– ref. Luz en la oscuridad: en busca de terapias para la ceguera hereditaria – https://theconversation.com/luz-en-la-oscuridad-en-busca-de-terapias-para-la-ceguera-hereditaria-278580

